ТОРБЕН ИНГЕМАНН ПЕТЕРСЕН, ЭйНАР ПАХЛА, ТОРБЬОРН ЗОММЕР и ТОМАС ЗИЛЛИНГ
Отдел Из Хирургия, Орхус Университет Больница, Орхус, Дания
Абстрактный.История вопроса: Есть только несколько отчетов о полной гастрэктомии с помощью лапароскопического хирургического подхода. Одним из объяснений является страх осложнений из-за анастомозной дегисценции при эзофаго-жеюнальном анастомозе, который, как известно, несет высокую заболеваемость и смертность. Внедрение степлеров способствовало тому, что анастомоз стал более безопасным и легким в выполнении, а также облегчило более продвинутую лапароскопическую хирургию. В открытой хирургии большинство хирургов используют циркулярный степлер для эзофаго-жеюнального анастомоза или технику наложения швов на руку. Оба метода трудно использовать в лапароскопической хирургии, особенно если пищевод узкий. Чтобы облегчить создание эзофаго-жевательных анастомозов, мы приняли технику с линейным сшитым анастомозом. Наш метод основан на технике сшивания, при которой пищевод разделяется над желудочной кардией, за которой следует эзофагойюностомия, выполняемая с помощью нового эндо Covidien GIA-60™Ультра универсальный степлер. Остаточное отверстие закрывают с помощью повторно рассасывающегося шва 3-0. Пациенты и методы: с июня 2009 года по май 2012 года 14 мужчин и 16 женщин (средний возраст = 66 лет, диапазон = 39-84 года) подверглись лапароскопической полной гастрэктомии из-за рака желудка. Результаты: Один пациент умер во время пребывания в больнице; соответствует послеоперационной смертности 3,3%. Утечка в эзофаго-жеюнальном анастомозе произошла у трех пациентов (10%). У двух пациентов с утечкой в эзофаго-жеюнальном анастомозе была дополнительная утечка двенадцатиперстной кишки, которая могла вызвать анастомотическую дегисценцию. Средняя продолжительность послеоперационного пребывания пациентов в стационаре составляла шесть дней (диапазон = 3-156 дней). Шесть пациентов перенесли повторную операцию из-за осложнений, в том числе одно эндоскопическое применение стента в анастомозе. Вывод: Несмотря на то, что скорость утечки 10% можно считать высокой, в этом исследовании описывается простой метод выполнения эзофаго-жеюностомии после гастрэктомии лапароскопическим подходом независимо от ширины пищевода. Это исследование также показывает, что лапароскопическая гастрэктомия может быть выполнена на более поздних стадиях рака желудка.
Переписка Для:Торбен Ингеманн Петерсен, доктор медицинских наук, отделение хирургической гастроэнтерологии L, Университетская больница Орхуса, Nørrebrogade 44, DK 8000 Åarhus C, Дания. Тел: + 45 78463889,
Факс: + 45 78462840 электронная почта: torbpete@rm.dk
Ключ Слова: Тотальная гастрэктомия, рак желудка, эзофаго-жеюнальный анастомоз, сшивающие устройства, малоинвазивная хирургическая техника.
0250-7005/2013 $2,00 + 0,40
После представления в 1994 году первого доклада КитаноИ др. Лапароскопической дистальной гастрэктомии при раке желудка (1) было зарегистрировано несколько случаев, в основном выполненных в Японии и Корее. Несмотря на экспоненциальное увеличение в год количества выполняемых лапароскопических процедур (2), ее принятие по сравнению с открытой процедурой остается спорным. Несмотря на растущий лапароскопический опыт и активность, лапароскопическая гастрэктомия остается исследовательской процедурой, почти исключительно предназначенной для раннего рака желудка и, по технической осуществимости, в основном выполняемой как лапароскопическая дистальная резекция желудка. Лапароскопический подход к более продвинутым ракам желудка еще предстоит дополнительно изучить, и процедура все еще приобретает более широкое признание, даже среди квалифицированных и опытных лапароскопистов. Эзофаго-жеюностомию выполнить нелегко, особенно если пищевод узкий. При открытой хирургии часто используется циркулярный степлер или техника наложения швов вручную. Эти методы не так просто использовать в лапароскопии, хотя есть новое устройство, OrVil™(Covidien, Mansfield, MA 02048, USA), где картридж кругового степлера соединен с желудочной трубкой для облегчения интубации эсфага через рот пациента. Помимо технических проблем, связанных с эзфагойюностомией, существует дискуссия относительно онкологической адекватности: возможно ли получить резекцию R0 и получить, по крайней мере, такое же большое количество резекционных лимфатических узлов, как иN открытая хирургия? (4) . Во-вторых, хотя несколько рандомизированных клинических испытаний сравнивали лапароскопическуюПротив Открытая гастрэктомия, крупномасштабные проспективные рандомизированные исследования с данными о долгосрочной выживаемости еще предстоит провести (5, 6). Наконец, лапароскопический подход является сложным и включает в себя длинную кривую обучения (2, 7). Попытка реализовать процедуру и приобрести технику занимает много времени и дорого, не в последнюю очередь в обработке повышенного возникновения осложнений на этапе обучения. В этом исследовании мы представляем результаты нашей серии последовательной лапароскопической тотальной гастрэктомии, где анастомоз применяется с помощью линейного сшивающего устройства, которое, как известно, создает значительно более широкий сшиваемый анастомоз по сравнению с круговым устройством (8).
Сбор данных о пациентах был одобрен Национальным управлением здравоохранения Дании. В период с июня 2009 года по май 2012 года 30 пациентов с подтвержденной биопсией опухолью желудка прошли лапароскопическую полную гастрэктомию в нашем отделении. Двадцать восемь пациентов имели подтвержденную биопсией карциному желудка, и у двух пациентов был метастатический рак в желудке: один пациент с предыдущим раком молочной железы и один пациент с предыдущим плоскоклеточным раком в области ротоглотки, оба с метастазированием желудка. Опухоли были расположены в верхней трети желудка у четырех пациентов, в средней трети у 10 пациентов и в нижней трети желудка у 12 пациентов. У четырех пациентов был пластический лиенит. Все пациенты прошли обширное обследование на отдаленное метастазирование, которое, в случае положительного результата, исключало пациента из операции. Предоперационная оценка включала гастроскопию с биопсией опухоли, лапароскопию и лапароскопическое ультразвуковое исследование, чтобы исключить распространение на соседние органы и посев брюшины, ФДГ-позитронно-эмиссионную томографию и компьютерное сканирование. Оперативность включала электрокардиограмму и при необходимости сердечные и легочные функциональные тесты. Пациенты со стадией опухоли ≥ T2N0 были отобраны для неоадъювантной химиотерапии (7). Характеристики пациентов приводятся в таблице I.
![]() Таблица I.Уголок пациентовХарактеристики.
Таблица I.Уголок пациентовХарактеристики.
• Количество пациентов 30 (3 пациента 2009, 9 пациентов 2010, 10 пациентов 2011, 8 пациентов 2012)
• Количество пациентов мужского/женского пола: 14/16
Возраст, медиана 66 (диапазон, 39-84) лет
• Индекс массы тела, медиана 23 (диапазон, 17-30)
• ASA-оценка, количество пациентов: ASA I 9, ASA II 19, ASA III 2
Хирургическая техника.Под общей анестезией пациент был помещен в положение лежа с раздвинутыми ногами и в легкое положение головы вверх. Хирурга поместили во французское положение между ногами пациента с помощником камеры на правой стороне пациента, а самый опытный помощник был на левой стороне пациента. На рисунке 1 показана оперативная процедура шаг за шагом. CO2 пневмоперитонеум индуцировали с помощью канулы Верреса, введенной в левое подреберье. Два 5-и два 12-мм порта были помещены в линию чуть выше пупка, а ретрактор печени Натасона был помещен в верхнюю часть эпигастрия, чтобы втянуть левую долю печени. Используя 30 ˚ вперед косой лапароскоп, брюшную полость обследовали на предмет перитонеального посева и метастазирования в печени после предоперационной химиотерапии. Удерживая левую долю печени в стороне, желудочно-печеночная связка была разделена с помощью ультразвуковых активированных ножниц (UltraCision Harmonic Scalpel®; Ethicon Endo-Surgery, LLC, Guaynabo, Пуэрто-Рико, США) после правой и левой диафрагмальной голени выше и вокруг пищевода, где френопищеводная связка и блуждающие нервы были разделены гармоническими ножницами. Затем гастроколическую связку разделяли вдоль границы поперечной толстой кишки, включая больший сальник в образце, который нужно резецировать. Диссекция проводилась справа до привратника, где инфрапилорический и супрапилорический лимфатические узлы (лимфатические станции 5 и 6 соответственно) были включены в резекцию. Правая желудочная артерия была разделена по своему происхождению от общей печеночной артерии гармоническими ножницами. Правая гастроэпиплоидная артерия и вена разделяются в их начале, где гастродуоденальная артерия выходит за привратник, либо с помощью нерассасывающихся зажимов, либо гармонических ножниц. Образец, который должен быть резефицирован, затем разделили ниже в двенадцатиперстной луковице чуть ниже привратника с помощью 60 мм Endo-Gia Duet.™, Коричневый магазин, среднего роста (Covidien) . Лимфатические узлы передней области гепатодуоЗатем резекцию денальной связки и лимфатических узлов в передней части общей печеночной артерии (станция 8 и станция 12 соответственно). Коронарная вена и левая желудочная артерия были разделены не реабсорбируемыми зажимами, где они появляются у основания ствола целиакии. Лимфатические узлы вдоль ствола целиакии и вдоль селезеночной артерии (станция 9 и станция 11) резекции гармоническими ножницами. Лимфатические узлы вдоль большей кривизны желудка были включены в резефицированные образцы, включая лимфатические узлы при большей кривизне желудка (станции 4a и 4b). Брюшная часть пищевода была мобилизована достаточно для резекции лимфатических узлов станции 1 и станции 2. Внутрибрюшной пищевод был пересечен 60 мм Endo-Gia.
Петля Roux-en-Y была подготовлена на 30 см ниже связки Treitz и анастомозированаАнте Колики Как боковая эзофа-гойджуностомия к задней стенке степлера закрыла внутрибрюшную часть пищевода 60 мм Endo-Gia 60, средней высоты. Непрерывно идущий реабсорбируемый шов 3-0 использовали, чтобы закрыть отверстие доступа сшитого анастомоза. В конце реконструкции желудочно-кишечного тракта анастомоз был протестирован на неэкспонированные утечки с метиленовым синим, введенным в анастомоз через транс-оральную трубку. Пятьдесят сантиметров дистально от эзофаго-жеюнального анастомоза, дистальный из стороны в сторону энтероанастомоз по Roux был выполнен с 60 мм Endo-Gia 60, средней высоты. Отверстие доступа закрывали с помощью повторно рассасывающегося шва 3-0 или V-образного фиксатора. Когда были выполнены два анастомоза, желчная нога в петле Roux-en-Y была разделена возле эзофаго-жеюностомии с 60-миллиметровым концом-Gia, коричневым магазином, средней высоты, были приняты меры, чтобы не пересекать петлю, чтобы близко к эзофаго-жеюностомии, избегая деваскуляризации кишечной ткани между двумя линиями степлера. Затем образец вставляли в мешок и извлекали через расширенное отверстие для порта. Наконец, 12-миллиметровые портовые отверстия были закрыты на уровне фасции с помощью повторно рассасывающегося шва. Кожа была закрыта степлером для кожи тела, Appose™ULC (Ковидьен, Мэнсфилд, Массачусетс, США).
Послеоперационный Уход. Пациентам давали 300 мл воды с нулевого дня. С 1 по 14 день пациентам была разрешена жидкая диета. Не использовались назогастральные трубки, катетер центральных мест или эпидуральный катетер. Анальгезия была ограничена чрескожной системой доставки фентанила и парацетамолом.
Было выполнено тридцать лапароскопических полных гастрэктомий. Кроме того, две процедуры были преобразованы в открытую гастрэктомию по показанию локально распространенного рака, включающего резекцию толстой кишки и спленэктомию в одном случае иПо показанию неясных границ резекции в другом случае. Классификация патологических опухолей-узлов-метастазов (pTNM) приведена в таблице II. Примечательно, что треть резекций включают пациентов со стадией IIb-III заболевания. Периоперационные результаты лапароскопической тотальной гастрэктомии перечислены в таблице III, а осложнения-в таблице IV.
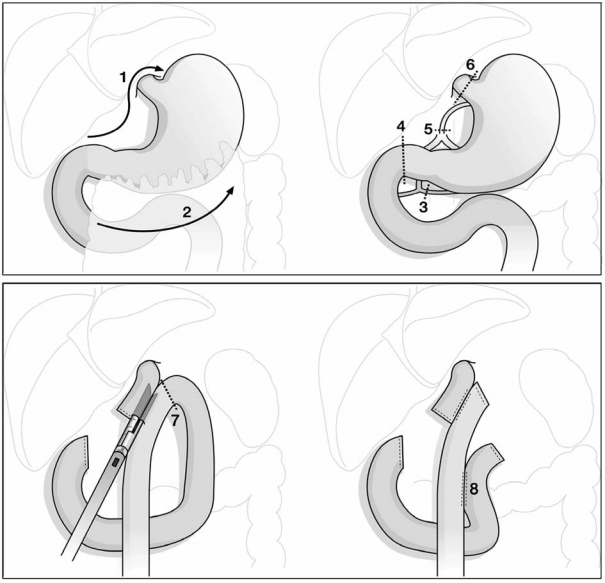
Диаграмма 1.Иллюстрация Из Оперативный Процедура: 1:Отдел Из Гепатогастральный Связка. 2:Мобилизация Из Желудочный Основные Кривизна Разделение Гастроколик Связка Включая Оментум В Резекция Образец. 3:Отдел Из Правый Гастроэпиплоический Артерия И Вена, Сбор урожая Лимфатические узлы Станция 5 И6. 4:Отдел Из Дуоденал Лампочка С A Линейный Степлер. 5:Отдел Из Корональный</Em>Вена И Слева Желудочный Артерия Закрыть Для Целиакия Багажник,Сбор урожая Лимфа Узлы Sation8,9И 11. 6: Резекция Из Пищевод В Гастроэзофагеальный Соединение В Пищевод Перерыв.
7:Выполнение Эзофагояджунал Анастомоз Сторона-Для-Сторона С 60Мм Эндо-ГИА. 8:Выполнение Ру-EN-Y Анастомоз Сторона-Для-Сторона С A60Мм Эндо-ГИА Приблизительно50См Из Гастроэзофагеальный Анастомоз На Алиментарный Багажник До Разделение Билиарный Багажник Просто Ниже Гастройджунал Анастомоз С Эндо-ГИА.
Было четыре пациента с радиологическими или клиническими признаками анастомозной утечки или признаками утечки из скошенного закрытия двенадцатиперстной кишки. Из трех пациентов с утечкой из эзофаго-жеюнального анастомоза у двух также была утечка из двенадцатиперстной кишки. У одного пациента была изолированная утечка из линии резекции двенадцатиперстной кишки. Другой пациент был повторно прооперирован в течение нескольких часов после операции из-за кровотечения из линии степлера в анастомозе Jejunojunal Roux-en-Y и обрабатывался с помощью лапароскопического применения гемостатического зажима. ОдинПациент был повторно прооперирован одну неделю после операции из-за грыжи тонкой кишки в пищеводном перерывах. В общей сложности у шести пациентов было серьезное осложнение, из которых пять потребовали повторной операции. Одно из основных осложнений лечилось консервативно с помощью эндоскопической вставки стента из пищевода для анастомотической утечки. Пациенты, которые приобрели серьезное осложнение, также ответственны за 75% зарегистрированных незначительных осложнений.
Таблица II.Патологическая Опухоль Узел Метастазирование Классификация (PTNM) .
PTNM | Количество пациентов |
PT1N0M0 | 5 |
PT1N1M0 | 1 |
PT2N0M0 | 6 |
PT2N1M0 | 5 |
PT2N2M0 | 3 |
PT2N3M0 | 1 |
PT3N0M0 | 1 |
PT3N1M0 | 1 |
PT3N2M0 | 1 |
PT3N3M0 | 1 |
PT4N1M0 | 1 |
PT4N3M0 | 1 |
Это исследование показывает, что минимально инвазивная полная гастрэктомия также может быть выполнена для более поздних стадий рака желудка, в отличие от большинства предыдущих исследований, где минимально инвазивные методы были ограничены ранним раком желудка (опухоли) в дистальной части желудка. Подход был дистальной резекции желудка в основном с использованием лапароскопически-ассистированного метода (2, 9) . Хирургический опыт в более продвинутом раке, подходящем для лапароскопической полной гастрэктомии, был ограничен, отчасти из-за скептицизма, и для этого есть несколько причин. Прежде всего из-за биологической природы желудочного сокаНЦР, где количество метастазов в лимфатические узлы имеет важное значение для прогнозирования прогноза.
Размер выборки в предыдущих рандомизированных клинических испытаниях был небольшим. Несмотря на то, что мета-анализ данных этих рандомизированных клинических испытаний был опубликован в последние годы, споры относительно безопасности с точки зрения осложнений, радикальной хирургии (резекция R0) и долгосрочной выживаемости все еще существуют (3, 4, 6) . Навыки, необходимые для проведения лапароскопической процедуры, востребованы хирургами с большим объемом опыта в лапароскопической хирургии. Кроме того, это требует хирургов со специальной подготовкой и интересом к лапароскопической хирургии желудка и включает в себя длинную кривую обучения (2, 10). Попытка реализовать процедуру и приобрести технику занимает много времени на этапе обучения.
Таблица III.Лапароскопическая Всего Гастрэктомия:Результаты Есть Дано Как Медиана с Диапазон .
Количество лимфатических узлов при диссекции Потеря крови, мл Время работы, мин Пребывание в больнице, дней | 23 (7-53) 100 (50-650) 180 (120-330) 6 (3-156) |
В предварительных данных от наших первых 30 процедур вЛапароскопическая полная гастрэктомия, представленная здесь, количество восстановленных лимфатических узлов в нашей лапароскопической резекции D1 приемлемо и полностью сопоставимо с таковым при открытой гастрэктомии (3, 11). Количество полученных лимфатических узлов было сопоставимо с данными, зарегистрированными в датском национальном регистре рака желудка относительно открытой тотальной гастрэктомии (7). Время операции было сопоставимо с нашим опытом в открытой хирургии. Из мета-анализа пациентов, перенесших резекцию D1-D2, ожидается, что оперативное время будет увеличено приблизительно на 60 минут, по меньшей мере, при лапароскопических дистальных резекциях, перенесших резекцию D2 (3) . Тем не менее, оперативное время было, по нашему опыту, сопоставимо с тем, что ожидается от открытой гастрэктомии, хотя это можно считать началом кривой обучения. Как и ожидалось, потеря крови была ограничена. Использование гармонического ультразвукового скальпеля имеет решающее значение для способности выполнять лапароскопическую гастрэктомию, хотя гастроэпиплоидная артерия и левая желудочная артерия были разделены после первого применения сосудистых зажимов к основанию сосудов. Продолжительность пребывания в больнице была сведена к минимуму при минимально инвазивной процедуре и, по оценкам, сократилась вдвое по сравнению с открытой операцией. Кроме того, удовлетворенность пациентов минимально инвазивной лапароскопической процедурой без осложнений была высокой в соответствии с рандомизированными клиническими исследованиями (12). Утечка произошла в двенадцатиперстной кишке у двух из трех пациентов с утечкой эзофагоеюностомии. Известно, что утечка двенадцатиперстной кишки, которая является одним из наиболее опасных осложнений, создает свищи по дуоденальному содержимому. Это может объяснить заживление поврежденной красной ткани при эзофаго-жеюностомии. Однако это также поднимает вопрос о достаточности герметизации степлером только разделенного двенадцатиперстного конца. Возможно, в нашем случае потребуется прошить двенадцатиперстную кишку прерванными повторно рассасываемыми швами. Переживание серьезного осложнения влечет за собой и другие осложнения, о чем свидетельствует высокая частота незначительных осложнений в этих предварительных данных.
Мы выбрали линейный сшиваемый анастомоз как для эзофаго-жеюностомии, так и для энтероанастомоза. Этот метод имеет несколько преимуществ перед круговым сшитым анастомозом (13). Прежде всего, он создает значительно более широкий анастомоз. Кроме того, это исключает проблему узкого пищевода или шва из кошелька, часто необходимого при круговом сшитом анастомозе. У нас не было утечки изАнастомоз Roux-en-Y, однако скорость утечки из верхнего анастомоза была высокой, что подчеркивает трудности при выполнении верхнего анастомоза. Известно, что пищевод имеет недостаточное кровоснабжение, и важно не препарировать слишком высоко в средостении, что приведет к деваскуляризации дистальной части пищевода.
Таблица IV.Лапароскопическая Всего Гастрэктомия: Осложнения Опытный.
Майор, 6 пациентов | Утечка из пищевода-жеюнального анастомоза Утечка двенадцатиперстной луковицы Послеоперационное кровотечение Грыжа в пищеводном перерывах | 3 3 1 1 |
Несовершеннолетние, 8 пациентов | Пневмония Пневмоторакс Кардиальная аритмия Абсцесс брюшной | 5 1 4 2 |
Лапароскопическая полная гастрэктомия, которая по-прежнему является спорной процедурой в отношении долгосрочной выживаемости, должна рассматриваться как процедура высокого риска и должна быть рассмотрена хирургическая безопасность. Лапароскопическая полная гастрэктомия является сложной и сложной процедурой. Кривая обучения длинная, и производительность процедуры требует, чтобы она была централизована в центрах большого объема. Японский опыт показывает, что эта лапароскопическая процедура выиграет от формализованной образовательной программы (14).
1 Китано S, Iso Y, Морияма M и Сугимати K: гастрэктомия Биллрот I при помощи лапароскопии. Surg лапароск эндоск4: 146- 148 1994.
Кодера Y, Fujiwara M, Ohashi N, Nakayama G, Koike M, Morita S и Nakao A: Лапароскопическая хирургия рака желудка: коллективный обзор с мета-анализом рандомизированных исследований. Дж Ам Колл Серг211(5): 677-685, 2010.
3 Вэй H, Вэй B, Qi C, Чен TF, Хуан Y, Чжэн, Хуан JL и Fang JF: лапароскопическаяПротив Открытая гастрэктомия с диссекцией лимфатических узлов D2 при раке желудка: мета-анализ. Surg Laparosc Эндоск Перкустан Tech21: 383-390, 2011.
4 Lee JH, Kim Y, Ryu KW, Lee JR, Kim CG, Choi IJ, Kook MC, Nam BH и Bae JM: II фаза клинического испытания лапароскопии при помощи дистальной гастрэктомии с диссекцией лимфатических узлов D2 для пациентов с раком желудка. Энн Сург Онкол14(11): 3148-3153, 2007.
5 Huscher CG, Минголи А, Сгарзини Г, Сансонетти А, Ди Паола М, Recher A и Понцано C: ЛапароскопическаяПротив Открытая субтотальная гастрэктомия для дистального рака желудка: результаты рандомизированного проспективного исследования за пять лет. Энн Сург241: 232-237, 2005.
Хаяси Х, Очиай Т, Шимада Х и Гунджи Y: Проспективное рандомизированное исследование открытыхVERSUS Лапароскопия-вспомогательная дистальная гастррекомия с экстраперигастральной диссекцией лимфатических узлов для раннего рака желудка. Сург эндоск19: 1172-1176, 2005.
7 ДЕЦВ. Национальные клинические рекомендации 2011. http:// gicancer.dk
8 Walther BS, Zilling T, Johnsson F, Stael von Holstein C и Joelsson B: Полная гастрэктомия и эзофагойюностомия с помощью линейных сшивающих устройств. Br J Surg76: 909-912, 1989.
9 Zeng YK, Yang ZL, Peng JS, Lin HS и Cai L: лапароскопия при помощиПротив Открытая дистальная гастрэктомия для раннего рака желудка доказательства из рандомизированных и нерандомизированных клинических испытаний. Энн Сург256: 39-52, 2012.
10 Shinohara T, Kanaya S, Taniguchi K, Fujita T, Yanaga K и Uyama I: Лапароскопическая полная гастрэктомия с диссекцией лимфатических узлов D2 при раке желудка. Арка Сург144(12): 1138-1142, 2009.
11 Huscher CG, Mingoli A, Sgarzini G, Sansonetti A, Lirici MM, Napolitano C и Piro F: Видеолапароскопическая общая и субтотальная гастрэктомия с расширенной диссекцией лимфатических узлов при раке желудка. Ам Дж Сург188(6): 728-735, 2004.
12 Kim YW, Baik YH, Yun YH, Nam BH, Kim DH, Choi IJ и Bae JM: Улучшение качества жизни после лапароскопической дистальной гастрэктомии при раннем раке желудка: результаты проспективного рандомизированного клинического исследования. Энн Сург248(5): 721-727, 2008.
13 Вальтер BS, Оскарсон JEA, Граффнер HO, Вальгрен S и Эвандер A: Esophagojejunostomy с EEA степлер. Хирургия99(5): 598-603, 1986.
14 Китано С и Ян H-K: Лапароскопическая гастрэктомия при раке. Springer Verlag, Нью-Йорк, ISBN 978-4-431-54002-1.
Получено Март 5, 2013Пересмотренный Мая22, 2013Приняты Мая 27, 2013
This is the first one.
This is the last one.